Artykuł powstał w ramach projektu pt.: „Wydawnictwa dla Amazonek”, który realizowany jest dzięki dofinansowaniu ze środków Państwowego Funduszu Rehabilitacji Osób Niepełnosprawnych

Rekonstrukcja wyniosłości piersiowej – czy istnieje obecnie standard postępowania?
1. Wstęp
Od ponad 50 lat posiadamy wyniki badań klinicznych, pokazujących, że, podstawową i najbardziej preferowaną metodą chirurgicznego leczenia raka piersi jest leczenie oszczędzające pierś. Terapia ta zapewnia stabilny, długoterminowy efekt estetyczny oraz, co być może istotniejsze, prowadzi do poprawy odległych wyników leczenie raka piersi (1). Nie zawsze jednak leczenie oszczędzające jest możliwe do przeprowadzenia i nadal mamy w onkologii sytuacje kliniczne, wymagające mastektomii – główne wskazania to wielkość guza (przekraczająca wielkość 25 procent objętości gruczołu), wieloośrodkowy charakter choroby, uniemożliwiający radykalne i z dobrym efektem kosmetycznym wycięcie wszystkich ognisk nowotworowych, czy obecność istotnych obciążeń genetycznych u pacjentki (głównie mutacja BRCA1). W takich sytuacjach często jedyną możliwą metodą leczenia chirurgicznego pozostaje mastektomia.
Jednocześnie o lat sześćdziesiątych XX wieku wprowadzenie implantów silikonowych znacząco poszerzyło możliwości chirurgii plastycznej i rekonstrukcyjnej, Dalszy, dynamiczny rozwój tych dziedzin na przełomie XX i XXI wieku oraz olbrzymi postęp w terapii raka gruczołu piersiowego z poprawą przeżywalności i zmniejszeniem liczby nawrotów miejscowych doprowadził do wyraźnego wzrostu satysfakcji pacjentek z wyników leczenia (2,3).
Rozwój technik rekonstrukcyjnych doprowadził do wzrostu oczekiwań estetycznych zarówno ze strony pacjentek, jak i chirurgów. Oczekiwania te stanowią istotną siłę napędową współczesnej chirurgii onkologicznej i związanej z nią działalności rekonstrukcyjnej, umożliwiając ciągłą poprawę wyników leczenia i jakości życia po terapiach onkologicznych.
Każdej pacjentce kwalifikowanej do mastektomii należy przedstawić możliwości rekonstrukcji piersi – zarówno w wariancie jednoczasowym (uwzględniając przebytą i planowaną terapię onkologiczną), jak i odroczonym – wykonywanym po zakończeniu terapii. Pamiętać należy przy tym, że nadal istnieją przeciwwskazania onkologiczne do rekonstrukcji jednoczasowej, takie jak diagnoza raka zapalnego przed leczeniem onkologicznym. Przy kwalifikacji do zabiegu konieczna jest ocena ogólnego stanu zdrowia chorej, chorób współistniejących oraz stosowanych leków. U pacjentek z cukrzycą należy dążyć do optymalnej kontroli glikemii, a palenie tytoniu powinno zostać bezwzględnie przerwane przed planowaną operacją.
Otyłość nie stanowi przeciwwskazania do rekonstrukcji wyniosłości piersiowej, jednak należy pamiętać, że istotnie zwiększa ryzyko powikłań pooperacyjnych (4,5).
Szczególną grupę stanowią pacjentki planowane do radioterapii pooperacyjnej oraz po radioterapii ściany klatki piersiowej. Radioterapia pooperacyjna jest uznawana za jeden z najważniejszych czynników pogarszających efekt kosmetyczny i funkcjonalny. Leczenie ro zwiększa ryzyko powikłań pooperacyjnych, ale przede wszystkim prowadzi do odległych powikłań związanych z naświetleniem rekonstruowanej wyniosłości piersiowej. Ocenia się, że ryzyko tego typu powikłań jest bardzo wysokie i sięga 40-50 % operowanych i poddanych naświetlaniu pacjentek (6–9). Z tego powodu potencjalne ryzyko powinno zostać szczegółowo omówione z pacjentką jeszcze przed rozpoczęciem leczenia chirurgicznego, optymalnie na początku planowania całej terapii raka piersi.
Do grupy podwyższonego ryzyka należą również chore po długotrwałym leczeniu systemowym przed operacją. U tych pacjentek często obserwuje się utratę masy mięśniowej i niedożywienie białkowe (sarkopenię), co może zwiększać częstość powikłań po zabiegach rekonstrukcyjnych wykonywanych jednoczasowo z mastektomią (10).
2. Rodzaje rekonstrukcji wyniosłości piersiowej
Współczesna chirurgia onkologiczna oferuje szeroki wachlarz metod rekonstrukcji piersi, dobieranych indywidualnie w zależności od:
- budowy anatomicznej pacjentki
- rodzaju i zaawansowania choroby
- preferencji chorej
Do najczęściej stosowanych metod rekonstrukcji należą:
- rekonstrukcja jednoczasowa z użyciem implantu lub ekspandera
- rekonstrukcja odroczona z użyciem implantu lub ekspandera
- rekonstrukcja z wykorzystaniem tkanek własnych (płaty tkankowe lub przeszczep tłuszczu)
3. Rekonstrukcja jednoczasowa z użyciem implantu lub ekspandera
Rekonstrukcja jednoczasowa wykonywana jest podczas tego samego zabiegu operacyjnego, bezpośrednio po przeprowadzeniu mastektomii. Procedura ta może być jednoetapowa lub dwuetapowa.
W przypadku rekonstrukcji jednoetapowej implant docelowy zostaje umieszczony w przestrzeni powstałej po usunięciu gruczołu piersiowego.
W niektórych sytuacjach – szczególnie przy niekorzystnych warunkach anatomicznych lub onkologicznych – konieczne jest zastosowanie procedury dwuetapowej. Dotyczy to m.in. sytuacji, gdy:
- tkanka podskórna jest bardzo cienka
- istnieje ryzyko niewystarczającego ukrwienia płatów skórnych (można ocenić to w trakcie zabiegu operacyjnego dzięki wykorzystaniu zieleni indocyjaniniowej i oceny przepływów tkankowych w płatach skórnych)
- guz znajduje się blisko skóry, co budzi wątpliwości co do radykalności chirurgicznej – wycięcie skóry jest konieczne, ponieważ stanowi ona onkologiczny margines wycięcia operacyjnego
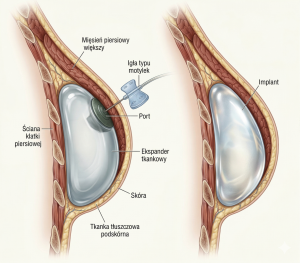
W takich przypadkach w pierwszym etapie wszczepiany jest ekspander tkankowy. Jest on formą czasowego implantu wyniosłości piersiowej, który stopniowo wypełnia się roztworem soli fizjologicznej w odstępach najczęściej 1–3 tygodniowych, aż do uzyskania odpowiedniego rozciągnięcia tkanek i uformowania wyniosłości piersiowej. Następnie ekspander wymieniany jest na implant ostateczny, co wymaga przeprowadzenia kolejnego zabiegu operacyjnego.
Należy podkreślić, że rekonstrukcja ma na celu odtworzenie wyniosłości piersiowej, nie jest to rekonstrukcja gruczołu piersiowego, który został wycięty w trakcie zabiegu operacyjnego. Ostateczny efekt kosmetyczny z reguły różni się od pierwotnego wyglądu własnego gruczołu piersiowego pod względem kształtu, konsystencji czy konturu odtwarzanej wyniosłości piersiowej. Implant jako ciało obce jest też zupełnie inaczej odczuwany przez kobiety. Dodatkowo implant nie odtwarza żadnej funkcji gruczołu piersiowego, takich jak czucie, odczuwanie temperatury czy pełne unerwienie operowanej okolicy.
Rycina 1. Różnica między ekspanderem a implantem
3.1. Techniczne aspekty rekonstrukcji jednoczasowej
Rodzaj cięcia skórnego i dobór techniki operacyjnej zależą od:
- kształtu piersi
- stopnia ptozy, czyli opadania piersi
- jakości tkanki podskórnej
- lokalizacji guza
Możliwe warianty operacyjne obejmują:
Skin-Sparing Mastectomy
Mastektomia podskórna z usunięciem kompleksu brodawka–otoczka oraz jednoczasową rekonstrukcją implantem lub ekspanderem. Ze względu na konieczność usunięcia większego fragmentu skóry najczęściej zabieg ten wykonywany jest z użyciem ekspandera.
Nipple-Sparing Mastectomy
Mastektomia podskórna z zachowaniem kompleksu brodawka–otoczka i jednoczasową rekonstrukcją implantem lub ekspanderem (ekspander zdecydowanie rzadziej).
Mastektomia z redukcją skóry (ang. skin-reducing mastectomy)
W tej technice zachowuje się kompleks brodawka–otoczka (najczęściej z przeniesieniem na szypule tkankowej lub jako przeszczep skórny) przy jednoczesnej redukcji nadmiaru skóry.
Do zabiegu takiego kwalifikowane są pacjentki ze znaczną ptozą (opadaniem) piersi, spełniające określone kryteria odległości brodawki od fałdu podpiersiowego oraz od wcięcia mostka – kryteria te ocenia chirurg przy kwalifikacji do zabiegu (11).
3.2. Położenie implantu
Implant może być umieszczony w dwóch głównych pozycjach:
- subpektoralnej – pod mięśniem piersiowym większym
- prepektoralnej – nad mięśniem piersiowym
Rycina 2. Różnice między położeniem prepektoralnym a subpektoralnym implantu i ekspandera.
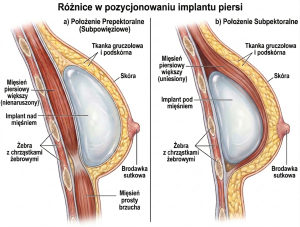
W ostatnich latach coraz częściej preferowane jest położenie prepektoralne. Pozwala ono uzyskać bardziej naturalny kształt wyniosłości piersiowej, ponieważ implant znajduje się w miejscu zbliżonym do anatomicznego położenia gruczołu piersiowego.
Ograniczeniem dla tej techniki mogą być jednak niekorzystne warunki anatomiczne, takie jak:
- niewystarczające ukrwienie płatów skórnych
- zbyt mała grubość tkanki podskórnej
W takich przypadkach konieczne może być zastosowanie dodatkowych technik wspomagających, np. lipotransferu, który może zmniejszyć rippling, czyli marszczenie tkanek na implancie, będący najczęstszym problemem po rekonstrukcji prepektoralnej. Na etapie kwalifikacji przy skrajnie małej grubości tkanki podskórnej, zaproponować można wykonanie od razu rekonstrukcji subpektoralnej (z wszystkimi jej konsekwencjami – mniej naturalna forma wyniosłości piersiowej oraz animacja, czyli widoczne kurczenie mięśnia piersiowego większego). Przy skrajnie nasilonym ripplingu proponować można także konwersję do przestrzeni subpektoralnej.
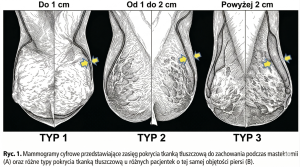
Rycina 3. Różne typy pokrycia tkanką tłuszczową gruczołu piersiowego, istotne przy kwalifikacji do zabiegu rekonstrukcji wyniosłości piersiowej.
4. Rekonstrukcja odroczona
Rekonstrukcja odroczona wykonywana jest po wcześniejszej mastektomii. W kwalifikacji do odpowiedniej metody bierze się pod uwagę przebyte leczenie onkologiczne – głównie radioterapię pooperacyjną ściany klatki piersiowej oraz jakość tkanek w loży po wcześniejszej amputacji gruczołu piersiowego (grubość tkanki podskórnej, jakość i mobilność blizny).
4.1. Rekonstrukcja odroczona z użyciem ekspandera lub implantu
Jest to podstawowa metoda rekonstrukcji wyniosłości piersiowej u pacjentek, które nie przeszły radioterapii. Najczęściej stosuje się w niej ekspander tkankowy wszczepiany pod mięsień piersiowy większy lub, przy dobrej jakości tkanek, podskórnie, tworząc przestrzeń prepektoralną.
Jest to procedura stosunkowo szybka i bezpieczna. Bardzo ostrożnie zastosować ją można u pacjentek po radioterapii, najczęściej, gdy jakość tkanek można poprawić poprzez zastosowanie lipotransferu (często kilkukrotnie przed zabiegiem wszczepienia ekspadnera).
4.2. Rekonstrukcja z użyciem tkanek własnych
U pacjentek po radioterapii wielu chirurgów preferuje rekonstrukcję z wykorzystaniem tkanek własnych, która znosi znaczną część ograniczeń technik implantowych. Podejście to ma olbrzymią przewagę po radioterapii, która znacząco pogarsza elastyczność i jakość tkanek.
Główną zaletą tej metody jest bardziej naturalne odczucie odtworzonej piersi, ponieważ jej objętość tworzą żywe, unaczynione tkanki pacjentki.
Wady dotyczą przede wszystkim miejsca dawczego, gdzie mogą powstawać:
- rozległe blizny
- opóźnione gojenie
Zabiegi te są bardziej czasochłonne i technicznie złożone, jednak ich długoterminowe efekty są często bardziej trwałe.
Najczęściej stosowane płaty to:
Płaty skórno-tłuszczowe
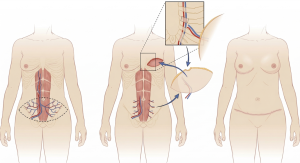
- DIEP (Deep Inferior Epigastric Perforator) – płat oparty na perforatorach tętnicy nabrzusznej dolnej głębokiej, pierś w całości odtworzona jest z tkanki własnej pacjentki, bez ubytków w funkcji mięśni, dodatkowo w uwagi na miejsce dawcze wykonywana jest plastyka brzucha (abdominoplastyka)
Rycina 4. Schemat ukazujący zasadę przygotowania i przeniesienia płata DIEP.
Płaty skórno-mięśniowe
- LD (Latissimus dorsi flap) – płat z mięśnia najszerszego grzbietu, jedna z najstarszych metod, która nadal znajduje miejsce w rekonstrukcji odroczonej, przy powikłaniach rekonstrukcji oraz powikłaniach leczenia onkologicznego. Minusem jest użycie mięśnia z osłabieniem pewnych funkcji kończyny górnej, w wybranych przypadkach możliwe alternatywy – płaty perforatorowe (np. TDAP – płat oparty na naczyniach wychodzących z tętnicy piersiowo-grzbietowej). Rekonstrukcja ta dla uzyskania pełnej objętości wyniosłości piersiowej najczęściej musi być wsparta wszczepieniem ekspandera lub implantu.
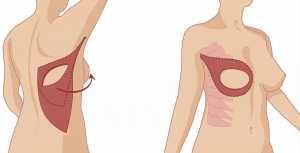
Rycina 5. Schemat ukazujący zasadę przygotowania i przeniesienia płata LD.
- TRAM (Transverse Rectus Abdominis Myocutaneous flap) – płat z mięśnia prostego brzucha, obecnie stosowany bardzo rzadko z uwagi na liczne problemy wczesne i odległe miejsca dawczego i biorczego.
Przeszczep tłuszczu własnego
Lipotransfer zyskuje coraz większą popularność zarówno wśród chirurgów, z uwagi na niewielkie obciążenie zabiegiem i powtarzalność procedury.
Do jego głównych zalet należą:
- niewielka inwazyjność
- niski odsetek powikłań
- krótki czas hospitalizacji
Metoda ta stosowana jest najczęściej do:
- poprawy grubości płatów skórnych po mastektomii
- korekcji defektów konturu po rekonstrukcji (12)
Prowadzone są także próby całkowitego odtworzenia wyniosłości piersiowej przy użyciu tłuszczu własnego lub w połączeniu z niewielkim implantem (13).
Główną wadą tej techniki jest znaczny stopień resorpcji przeszczepionego tłuszczu (25–52%), co często wymaga powtórzenia zabiegu (14).
5. Powikłania po zabiegach rekonstrukcyjnych
Powikłania można podzielić na:
Powikłania wczesne
- zakażenie implantu
- martwica skóry i odsłonięcie implantu
- krwiaki
- surowiczaki (wyciek lub gromadzenie się płynu)
Powikłania późne
- przykurcz torebkowy
- przewlekły ból
- przemieszczenie lub rotacja implantu
- pęknięcie implantu
Do rzadkich powikłań późnych należą:
BIA-ALCL
Breast Implant‑Associated Anaplastic Large‑Cell Lymphoma – chłoniak z komórek T związany z implantami piersi. Ryzyko jego wystąpienia wynosi około 1:3000–1:130000 i dotyczy głównie implantów teksturowanych.
ASIA
Autoimmune/Autoinflammatory Syndrome Induced by Adjuvants – zespół autoimmunologiczny związany prawdopodobnie z reakcją na silikon lub inne substancje zawarte w implantach. Mechanizm jego powstawania pozostaje jednak nie w pełni poznany i wymaga dalszych badań (15).
6. Podsumowanie
Podsumowując, zabiegi rekonstrukcyjne wyniosłości piersiowej to złożony problem. Kwalifikacja do zabiegów oraz przebieg procesu rekonstrukcji to sprawa mocno zindywidualizowana i zależna przede wszystkim od aspektów leczenia onkologicznego. Często decyzja o rekonstrukcji wymaga wielu analiz i kilku spotkań z chirurgiem, aby wybrać najlepszą opcję, która nie zaburzy schematu najważniejszego – planowego rozpoczynania kolejnych etapów terapii. W kwalifikacji do rekonstrukcji kierować się należy przede wszystkim dobrem pacjentki i szczegółowo omówić wszystkie konsekwencje wczesne i odległe rekonstrukcji, rozpatrując każdy przypadek indywidualnie. Każda niewłaściwa decyzja może przełożyć się na gorszy wynik leczenia, a tego należy unikać. Dlatego w wybranych przypadkach decyzja o rekonstrukcji odroczonej jest opcją najbezpieczniejszą, decyzja podejmowana jest wtedy na spokojnie, po analizie całości przebytej terapii, która najczęściej już się zakończyła.
Bibliografia
- De la Cruz Ku G, Karamchandani M, Chambergo-Michilot D i wsp. Does Breast-Conserving Surgery with Radiotherapy have a Better Survival than Mastectomy? A Meta-Analysis of More than 1,500,000 Patients. Ann Surg Oncol 2022; 29(10):6163-6188.
- Ryu JM, Paik HJ, Park S, et al. Oncologic outcomes after immediate breast reconstruction following total mastectomy in patients with breast cancer: a matched case-control study. J Breast Cancer. 2017;20:74–81.
- Chang JM, Kosiorek HE, Dueck AC, et al. Trends in mastectomy and reconstruction for breast cancer; a twelve year experience from a tertiary care center. Am J Surg. 2016;212:1201–1210.
- Huo J, Smith BD, Giordano SH, Reece GP, Shih YT. Postmastectomy breast reconstrction and its subsequent complications: A comparison between obese and non-obese women with breast cancer. Breast Cancer Res Treat. 2016;157:373–383.
- McCarthy CM, Mehrara BJ, Riedel E, et al. Predicting complications following expander/implant breast reconstruction: An outcomes analysis based on preoperative clinical risk. Plast Reconstr Surg. 2008;121:1886–1892.
- Reish RG, Lin A, Phillips NA, et al. Breast reconstruction outcomes after nipple-sparing mastectomy and radiation therapy. Plast Reconstr Surg. 2015;135:959–966.
- Nelson JA, Disa JJ. Breast reconstruction and radiation therapy: An update. Plast Reconstr Surg. 2017;140(5S Advances in Breast Reconstruction):60S–68S.
- Weichman KE, Cemal Y, Albornoz CR, et al. Unilateral preoperative chest wall irradiation in bilateral tissue expander breast reconstruction with acellular dermal matrix: A prospective outcomes analysis. Plast Reconstr Surg. 2013;131:921–927.
- Jagsi R, Jiang J, Momoh AO, et al. Complications after mastectomy and immediate breast reconstruction for breast cancer: A claims-based analysis. Ann Surg. 2016;263:219–227.
- Seth I, Bulloch G, Jennings M, et al. The effect of chemotherapy on the complication rates of breast reconstruction: A systematic review and meta-analysis. J Plast Reconstr Aesthet Surg. 2023 Jul;82:186-197.
- Nava MB, Cortinovis U, Ottolenghi J, Riggio E, Pennati A, Catanuto G, et al. Skin-reducing mastectomy. Plast Reconstr Surg. 2006;118:603–10.
- Auclair E., Anavekar N. Combined Use of Implant and Fat Grafting for Breast Augmentation. Clin. Plast. Surg. 2015;42:307–314. doi: 10.1016/j.cps.2015.03.005.
- Stillaert F.B.J.L., Lannau B., Van Landuyt K., Blondeel P.N. The Prepectoral, Hybrid Breast Reconstruction: The Synergy of Lipofilling and Breast Implants. Plast. Reconstr. Surg. Glob. Open. 2020;23:e2966.
- Kim H.Y., Jung B.K., Lew D.H., Lee D.W. Autologous Fat Graft in the Reconstructed Breast: Fat Absorption Rate and Safety based on Sonographic Identification. Arch. Plast. Surg. 2014;41:740–747. doi: 10.5999/aps.2014.41.6.740.
- Colaris MJL, de Boer M, van der Hulst RR, Cohen Tervaert JW. Two hundreds cases of ASIA syndrome following silicone implants: a comparative study of 30 years and a review of current literature. Immunol Res. 2017 Feb;65(1):120-128. doi: 10.1007/s12026-016-8821-y. PMID: 27406737; PMCID: PMC5406475.
Autor: dr n.med. Piotr Nowaczyk, specjalista chirurgii ogólnej, specjalista chirurgii onkologicznej, na co dzień pracuje na Oddziale Chirurgii Onkologicznej Chorób Piersi w Wielkopolskim Centrum Onkologii w Poznaniu. Badacz, współbadacz i koordynator w zakresie projektów naukowych i badań klinicznych obejmujących raka piersi, raka żołądka, raka odbytnicy oraz problematykę leczenia żywieniowego w onkologii.



